những kiến thức về nguyên tử khối rất đặc trưng vì bọn chúng sẽ đi theo những em suốt 3 năm THPT. Biết được tầm đặc trưng đó, quanangiangghe.com đang tổng hợp kiến thức và kỹ năng về nguyên tử khối cùng bộ bài bác tập từ bỏ luận rất hấp dẫn và ý nghĩa. Các em cùng theo dõi bài viết dưới trên đây nhé!
1. Nguyên tử khối là gì?
1.1. Khái niệm
Khối lượng của một nguyên tử được tính bằng đvC được điện thoại tư vấn là nguyên tử khối. Sẽ sở hữu được các nguyên tử khối khác biệt giữa các nguyên tố không giống nhau.
Bạn đang xem: Nguyên tử khối của nitơ
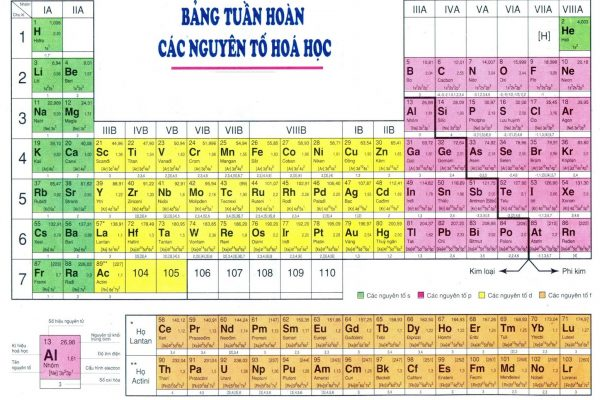
KL của một nguyên tử chính bằng tổng KL của những thành phần tạo nên nguyên tử đó (p, e, n) nhưng bởi hạt e tất cả KL quá bé so cùng với tổng KL buộc phải ta coi KL của phân tử e = 0. Bởi vì đó, lúc xét mang lại KL nguyên tử, ta xem như KL nguyên tử bằng tổng KL của hạt phường và n có ở trong phân tử nhân của nguyên tử (m = mp + mn)
VD: Nguyên tử khối của Ag là 108 cùng nguyên tử khối của Mg là 24
1.2. Đơn vị của nguyên tử khối là gì?
Trong thực tế, nguyên tử tất cả KL vô cùng nhỏ bé, nếu tính dựa trên g thì số trị rất nhỏ tuổi và khó khăn sử dụng.
VD: KL của một nguyên tử C là 0, 000 000 000 000 000 000 000 019 926 g (hay hoàn toàn có thể viết ngắn lại hơn = 1,9926.10-23g). Vị đó, những nhà kỹ thuật đã nghĩ về ra một cách khác giúp biểu lộ KL của nguyên tử. Thế thể, họ đã quy ước rằng lấy 1/12 cân nặng của nguyên tử C để làm đơn vị bình thường KL cho nguyên tử - đơn vị C, viết tắt là đvC. Nhưng ký hiệu nước ngoài để biểu đạt nó lại là “u”. Dựa trên đơn vị này, chúng ta cũng có thể tính KL của một nguyên tử một biện pháp dễ dàng.
1.3. Nguyên tử khối trung bình
Hầu hết những nguyên tố hóa học đều tồn tại ở dạng lếu hợp của rất nhiều đồng vị với tỉ lệ thành phần % số nguyên tử xác định. Do vậy, nguyên tử khối của các nguyên tố mà có không ít đồng vị đã được khẳng định là nguyên tử khối TB của lếu láo hợp những đồng vị đó gồm tính phụ thuộc tỉ lệ % số nguyên tử tương ứng. Trả sử là A cùng B là 2 đồng vị của mẫu A và B. Kí hiệu A cùng B theo thứ tự là nguyên tử khối của 2 đồng vị với tỉ lệ % số nguyên tử tương ứng là a và b. Lúc ấy nguyên tử khối TB, kí hiệu Atb của yếu tố X là:
Atb = (a.A + b.B)/100
2. Bảng nguyên tử khối chi tiết các nguyên tố
Để chúng ta dễ dàng tra cứu cùng tổng hợp những kiến thức có ích khác, quanangiangghe.com sẽ share lại bảng nguyên tử khối cụ thể của những nguyên tố hóa học.
STT | Tên nguyên tố | Ký hiệu hóa học | Nguyên tử khối |
1 | Hiđro | H | 1 |
2 | Heli | He | 4 |
3 | Liti | Li | 7 |
4 | Beri | Be | 9 |
5 | Bo | B | 11 |
6 | Cacbon | C | 12 |
7 | Nitơ | N | 14 |
8 | Oxi | O | 16 |
9 | Flo | F | 19 |
10 | Neon | Ne | 20 |
11 | Natri | Na | 23 |
12 | Magie | Mg | 24 |
13 | Nhôm | Al | 27 |
14 | Silic | Si | 28 |
15 | Photpho | P | 31 |
16 | Lưu huỳnh | S | 32 |
17 | Clo | Cl | 35,5 |
18 | Argon | Ar | 39,9 |
19 | Kali | K | 39 |
20 | Canxi | Ca | 40 |
21 | Scandi | Sc | 44.955912(6) |
22 | Titan | Ti | 47,867(1) |
23 | Vanadi | V | 50,9415(1) |
24 | Crom | Cr | 51,9961(6) |
25 | Mangan | Mn | 54,938044 |
26 | Sắt | Fe | 55,845 |
27 | Coban | Co | 58,933195 |
28 | Niken | Ni | 58,6934 |
29 | Đồng | Cu | 63,546 |
30 | Kẽm | Zn | 65,38 |
31 | Gali | Ga | 69,723 |
32 | Gecmani | Ge | 72,64 |
33 | Asen | As | 74,9216 |
34 | Selen | Se | 78.96 |
35 | Brom | Br | 79,904 |
36 | Kryton | Kr | 83,798 |
37 | Rubidi | Rb | 85,4678 |
38 | Stronti | Sr | 87,62 |
39 | Yttri | Y | 88,90585 |
40 | Zicorni | Zr | 91,224 |
41 | Niobi | Nb | 92,90638 |
42 | Molypden | Mo | 95,95 |
43 | Tecneti | Tc | 98 |
44 | Rutheni | Ru | 101,07 |
45 | Rhodi | Rh | 102,9055 |
46 | Paladi | Pd | 106,42 |
47 | Bạc | Ag | 107,8682 |
48 | Cadmi | Cd | 112,411 |
49 | Indi | In | 114,818 |
50 | Thiếc | Sn | 118,71 |
51 | Antimon | Sb | 121,76 |
52 | Telua | Te | 127,6 |
53 | I ốt | I | 126,90447 |
54 | Xenon | Xe | 131,293 |
55 | Xêsi | Cs | 132,90545 |
56 | Bari | Ba | 137,327 |
57 | Lantan | La | 138,90547 |
58 | Xeri | Cs | 140,116 |
59 | Praseodymi | Pr | 140,90765 |
60 | Neodymi | Nd | 144,242 |
61 | Promethi | Pm | 145 |
62 | Samari | Sm | 150,36 |
63 | Europi | Eu | 151,964 |
64 | Gadolini | Gd | 157,25 |
65 | Terbi | Tb | 158,92535 |
66 | Dysprosi | Dy | 162,5 |
67 | Holmi | Ho | 164,93032 |
68 | Erbi | Er | 167,259 |
69 | Thuli | Tm | 168,93421 |
70 | Ytterbium | Yb | 173,04 |
71 | Luteti | Lu | 174,967 |
72 | Hafni | Hf | 178,49 |
73 | Tantal | Ta | 180,94788 |
74 | Wolfram | W | 183,84 |
75 | Rheni | Re | 186,207 |
76 | Osmi | Os | 190,23 |
77 | Iridi | Ir | 192,217 |
78 | Platin | Pt | 195,084 |
79 | Vàng | Au | 196,96657 |
80 | Thủy ngân | Hg | 200,59 |
81 | Tali | TI | 204,3833 |
82 | Chì | Pb | 207,2 |
83 | Bitmut | Bi | 208,9804 |
84 | Poloni | Po | 209 |
85 | Astatin | At | 210 |
86 | Radon | Rn | 222 |
87 | Franxi | Fr | 223 |
88 | Radi | Ra | 226 |
89 | Actini | Ac | 227 |
90 | Thori | Th | 232,03806 |
91 | Protactini | Pa | 231,03588 |
92 | Urani | U | 238,02891 |
93 | Neptuni | Np | 237,0482 |
94 | Plutoni | Pu | 244 |
95 | Americi | Am | 243 |
96 | Curi | Cm | 247 |
97 | Berkeli | Bk | 247 |
98 | Californi | Cf | 251 |
99 | Einsteini | Es | 252 |
100 | Fermi | Fm | 257 |
101 | Mendelevi | Md | 258 |
102 | Nobeli | No | 259 |
103 | Lawrenci | Lr | 262 |
104 | Rutherfordi | Rf | 267 |
105 | Dubni | Db | 268 |
106 | Seaborgi | Sg | <269> |
107 | Bohri | Bh | <270> |
108 | Hassi | Hs | <269> |
109 | Meitneri | Mt | <278> |
110 | Darmstadti | Ds | <281> |
111 | Roentgeni | Rg | <281> |
112 | Copernixi | Cn | <285> |
113 | Nihoni | Nh | <286> |
114 | Flerovi | Fl | <289> |
115 | Moscovi | Mc | <288> |
116 | Livermori | Lv | <293> |
117 | Tennessine | Ts | <294> |
118 | Oganesson | Og | <294 |
3. Biện pháp tính trọng lượng thực của nguyên tử
Có thể phân tích và lý giải một cách đơn giản dễ dàng là vì cân nặng nguyên tử tính bằng gam có mức giá trị khôn cùng nhỏ, ko tiện trong câu hỏi tính toán. Nên bạn ta quy mong lấy 1/12 KL nguyên tử C làm đơn vị KL nguyên tử (đvC).
Tuy nhiên, quá trình tính KL bằng g của các nguyên tử chưa phải là không thực hiện được. Trọng lượng tính bởi g đó đó là KL thực của nguyên tử.
Bước 1: Cần ghi nhớ giải pháp quy đổi 1 đvC = 0,166.10-23 (g)
Bước 2: Tra bảng kiếm tìm nguyên tử khối của nguyên tố và nỗ lực học thuộc bài ca nguyên tử khối chẳng hạn nguyên tố A có NTK là a, tức A = a.
Bước 3: cân nặng thực của thành phần A: mA=a . 0,166 . 10-23 = ? (g)
4. Phương thức học nằm trong bảng nguyên tử khối vô cùng dễ nhớ
4.1. Học thuộc lòng bằng flashcards

Đây cũng chính là một phương pháp học tập cực kỳ hay, các em có thể ôn luyện hàng ngày và tăng thời hạn cho nó bằng cách dùng flashcard.
4.2. Bài xích ca nguyên tử khối
Anh hydro là 1 trong những (1)
Mười hai (12) cột carbon
Nitro mười tứ (14) tròn
Oxi mỏi mòn mười sáu (16)
Natri xuất xắc láu táu
Nhảy tót lên hai tía (23)
Khiến Magie ngay sát nhà
Ngậm ngùi đành hai tứ (24)
Hai bảy (27) nhôm la lớn
Lưu huỳnh giành ba hai (32)
Khác người thật là tài
Clo cha lăm rưỡi (35,5)
Kali thích tía chín (39)
Canxi tiếp tư mươi (40)
Năm lăm (55) mangan cười
Sắt trên đây rồi năm sáu (56)
Sáu tư (64) đồng nổi cáu
Bởi yếu kẽm sáu lăm (65)
Tám mươi (80) Brom nằm
Xa bội bạc trăm lẻ tám (108)
Bari lòng bi ai chán
Một tía bảy (137) ích chi
Kém fan ta còn gì
Hai lẻ bảy (207) chưng chì
Thủy ngân hai lẻ một (201)…
5. Một trong những ứng dụng của bảng nguyên tử khối xuất xắc phân tử khối trong những bài tập hóa học
Bảng nguyên tử khối sẽ đem về cho bọn họ tính ứng dụng rất to lớn trong bộ môn hóa học, nhất là phần kỹ năng của hóa vô cơ. Hầu như các bài xích tập hóa học hầu như phải sử dụng bảng này.
Tìm nguyên tố sinh hoạt trong phù hợp chất
Đối cùng với những bước làm quen đầu tiên với cỗ môn hóa học, đây là một một trong những dạng bài xích tập phổ biến nhất. Một VD minh họa solo giản: Hợp hóa học của kim loại A kết hợp với axit H2SO4 sẽ tạo nên ra muối với bí quyết là A2SO4. Tổng phân tử khối của hợp hóa học này đang rơi vào mức 160 đvC. Xác định được yếu tắc A là gì. Ta có thể dễ dàng giải so với các vấn đề này như sau:
Dựa vào bảng nguyên tử khối ta có:
Nguyên tử khối của S bằng: 32
Nguyên tử khối của oxy bởi : 16
Theo công thức hợp hóa học phía trên, ta gồm A+32+16x4=160 => A=64.
Dựa vào bảng nguyên tử khối thì nguyên tử khối của Đồng được. Vậy yếu tố đề bài bác cần tìm đó là đồng (Cu).
Tìm nguyên tố khi biết nguyên tử khối
Đối với các dạng bài xích tập solo giản, những em sẽ thường xuyên phát hiện một số câu hỏi như là xác định nguyên tố tất cả nguyên tử khối gấp gấp đôi so với oxy.
Để có tác dụng được bài xích tập liên quan đến phần này, những em đề nghị ghi lưu giữ được nguyên tử khối của oxi là 16, yếu tố với nguyên tử khối gấp gấp đôi oxi gồm nguyên tử khốii là 32. Vậy nên ta hoàn toàn có thể nhận ra một cách dễ ợt → lưu giữ huỳnh
Các dạng bài tập được nêu ở trên có giữa những dạng đơn giản và dễ dàng và cơ phiên bản nhất của hóa học ở bậc trung học. Mặc dù nhiên, trước khi đi làm việc việc và mày mò kĩ rộng về hóa, những em cũng cần được ghi ghi nhớ được các kiến thức cơ phiên bản nhất để sở hữu một bắt đầu suôn sẻ với một gốc rễ thật bền vững nhé.
6. Bài tập luyện tập về nguyên tử khối
Câu 1: Một nguyên tử nhôm (kí hiệu là Al) có chứa 13 p, 13 e với 14 n. Hãy khẳng định KL của một nguyên tử nhôm.
Lời giải
Ta gồm mp = 13 . 1,6726 . 10-24 = 2,174.10-23 = 21,74.10-24 g
mn = 14 . 1,675 . 10-24 = 2,345.10-23 = 23,45.10-24 g
me = 13 . 9,1 . 10-28 = 1,183 . 10-26 = 0,01183 . 10-24 g
=> KL 1 nguyên tử nhôm được tính là: mp + mn + me = 21,74.10-24 + 23,45.10-24 + 0,01183 . 10-24 = 45,19 . 10-24 g
Câu 2: Hãy cho biết thêm giữa nguyên tử magie với cacbon thì nguyên tử nào nặng hay khối lượng nhẹ hơn bao nhiêu lần?
Lời giải
Nguyên tử khối của Mg theo luồng thông tin có sẵn là 24 đvC; nguyên tử khối của C là 12 đvC.
⇒ Nguyên tử Mg nặng rộng C với nặng 2412=2 (lần)
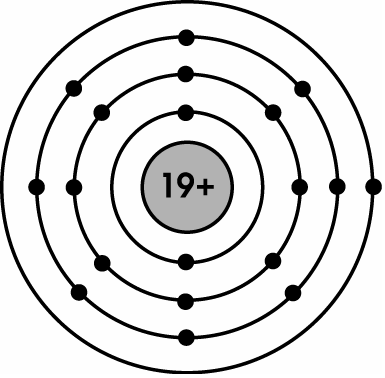
Câu 3: Hãy vẽ kết cấu của nguyên tử X nhưng mà trong phân tử nhân của nguyên tử X gồm chứa 19 p.
Lời giải
Vì nguyên tử có đặc thù trung hòa về điện đề xuất ta gồm số e = số phường = 19
=> Lớp 1 gồm 2 e, lớp 2 gồm 8 e, lớp 3 có 8 e với lớp 4 có 1 e
Ta gồm sơ đồ:
Câu 4: Nguyên tử X nặng cấp 4 lần nguyên tử nitơ. Tính nguyên tử khối của X và hãy cho biết nó là thành phần nào?
Lời giải
Nguyên tử khối của Nito = 14 đvC
⇒ Nguyên tử khối của yếu tắc X = 4 . 14 = 56 (đvC)
Vậy X là yếu tố sắt (Fe).
Câu 5: KL kha khá của một phân tử H2O là
Lời giải
KL kha khá của một phân tử H2O = MH2O = 2.1 + 16 = 18 (đvC).
Câu 6: hiểu được 4 nguyên tử Mg nặng bằng 3 nguyên tử của yếu tố X. Vậy X là nguyên tố nào?
Lời giải
24 đvC là nguyên tử khối của Mg. Đặt nguyên tử khối của X chính bởi M.
Theo đề bài, ta có: 4 . 24 = 3 . M ⇒ M = (4 . 24)/3 = 32 đvC
Vậy X chính là nguyên tố diêm sinh (kí hiệu S).
Câu 7: Một hợp hóa học được tạo thành vì chưng 2 nguyên tử Oxi liên kết với 1 nguyên tử X. Hiểu được hợp chất này còn có phân tử khối khối nặng hơn phân tử hiđro 22 lần.
a) tìm kiếm phân tử khối hợp hóa học đó
b) tìm nguyên tử khối của X và từ đó cho thấy tên nguyên tố với kí hiệu hóa học
Lời giải
Phân tử hidro tất cả công thức chất hóa học là H2 => MH2 = 2 . 1 = 2 (đvC)
Theo đầu bài:
Hợp chất nặng hơn phân tử H 22 lần.
Xem thêm: App Selfie Đẹp Cho Nam - 10+ Phần Mềm, Ứng Dụng Chụp Ảnh Đẹp Miễn Phí
=> M = 2.22 = 44
1 nguyên tử X link với 2 nguyên tử O tạo thành hợp chất (1X; 2O)
Nên ta có: M = X + 2.16 = X + 32
Mà bên trên chúng ta đã kiếm được M = 44
=> X + 32 = 44
=> X = 44 – 32 = 12
Vậy X là yếu tắc cacbon (C)
Câu 8: Đồng tất cả 2 đồng vị là 6329Cu cùng 6529Cu. Nguyên tử khối vừa đủ của Cu bằng 63,54. Thành phần tỷ lệ số nguyên tử của từng đồng vị bằng bao nhiêu?
Lời giải
Đặt thành phần tỷ lệ của 6329Cu là x (%)
Suy ra thành phần phần trăm của đồng vị 6529Cu là 1 trong - x (%)
Ta có
M = 63.x + 65(1-x) = 63,54
63x-65x =63,54-65
-2x = 1,46
x =0,73(%)
⇒ % 6329Cu = 73% với % 6529Cu = 27%
Câu 9: vào tự nhiên, X có hai đồng vị 3517X cùng 3717X, chiếm phần lần lượt 75,77% với 24,23% số nguyên tử X. Y gồm hai đồng vị à 11Y với 21Y, chiếm phần lần lượt 99,2% và 0,8% số nguyên tử Y.
a) Trong tự nhiên tồn tại từng nào loại phân tử XY?
b) Phân tử khối mức độ vừa phải của phân tử XY bằng bao nhiêu?
Lời giải
a) Số loại phân tử XY tất cả trong tự nhiên và thoải mái là: 35X -1Y, 35X -2Y, 37X -1Y, 37X -2Y
b) Nguyên tử khối TB của X là 75,77.35 + 24,23.37100 = 35,485
Nguyên tử khối TB của X là: 99.2,1 + 0.8.2100 = 1,008
Phân tử khối TB của XY: 35,485 + 1,008 = 36,493 = 36,5
Câu 10: yếu tố Cl có 2 đồng vị bền trong thoải mái và tự nhiên bao gồm: 3717Cl chiếm phần 24,23% tổng thể nguyên tử, còn lại là 3517Cl. Nguyên tố % theo KL của 3717Cl trong HClO4 là bao nhiêu?
Lời giải:
Ta có: % 3717Cl = 24,23% ⇒ % 3517Cl = 100% - 24,23% = 75,77%
ACl = 37.24,23 + 35.75,77100 = 35,4846
⇒ tỷ lệ đồng vị 3517Cl trong HClO4 là:
37.24,23%1+ 35,4846 + 16,4.100=8,92%
Kiến thức về nguyên tử khối sẽ luôn đi theo những em xuyên suốt nên yên cầu các em đề xuất nhớ được bảng nguyên tử khối và vận dụng được nó vào các bài tập. quanangiangghe.com sẽ giúp những em học giỏi hơn phần này bằng cách tổng hợp cô đọng lý thuyết và bài xích tập về phần này. Để học thêm được nhiều các kỹ năng và kiến thức hay cùng thú vị về Hoá học 10 cũng tương tự Hoá học trung học phổ thông thì những em hãy truy vấn quanangiangghe.com hoặc đk khoá học với các thầy cô quanangiangghe.com ngay bây giờ nhé!